Aifa agli allergici: possibile presenza di lattice in alcuni vaccini
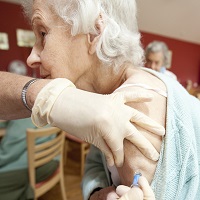
L'avviso pubblicato riguarda solo il confezionamento dei vaccini antinfluenzali. Nessuna contaminazione
Anche quest’anno l’AIFA ha condotto un approfondimento con le Aziende titolari di Autorizzazione all’Immissione in Commercio (AIC) sulla presenza di lattice/latex/gomma naturale nelle diverse componenti delle siringhe pre-riempite (es. cilindro, pistone, cappuccio protettivo copri ago, copri punta, ecc.) o degli applicatori nasali dei vaccini anti-influenzali autorizzati per la stagione 2019-2020.
Tale informazione risulta infatti di estrema importanza per i soggetti allergici al lattice che necessitano della copertura vaccinale, i quali, in caso di presenza di lattice anche in tracce, sarebbero esposti al rischio di reazioni allergiche.
pubblicità
"L'avviso pubblicato riguarda solo il confezionamento dei vaccini antinfluenzali a tutela di coloro che presentano allergie a tale sostanza. Ciò per consentire anche ai soggetti allergici una adeguata vaccinazione informandoli sui prodotti latex-free. Nessuna contaminazione dunque nei vaccini antinfluenzali".
La “Linea guida della Commissione Europea sugli eccipienti nell’etichettatura e nel foglio illustrativo dei medicinali” prevede l’inserimento di un’avvertenza nel Foglio Illustrativo nel caso in cui il lattice sia presente in qualsiasi quantità, indipendentemente dalla via di somministrazione del medicinale. In caso di assenza di lattice, invece, non è richiesto l’inserimento di specifiche dichiarazioni.
L’AIFA ha comunque ritenuto opportuno contattare tutte le Aziende titolari dell’AIC dei vaccini anti-influenzali autorizzati in Italia, chiedendo di certificare, laddove non specificato nel Riassunto delle Caratteristiche del Prodotto (RCP) e nel Foglio Illustrativo, la presenza di lattice nelle componenti dei confezionamenti primari.
Sulla base delle dichiarazioni dei titolari delle AIC e di quanto riportato nell’RCP/FI di questi vaccini, l’AIFA fornisce quindi le seguenti informazioni di riepilogo allo scopo di contribuire ulteriormente all'uso sicuro e corretto dei vaccini anti-influenzali stagionali anche nei soggetti con storia di reazioni allergiche severe al lattice:
| Titolare di AIC | Nome commerciale del vaccino | Presenza di lattice nel confezionamento primario |
| Mylan IRE HEALTHCARE LIMITED | Influvac S tetra | Non contiene lattice – non si può escludere la possibilità che, durante il processo produttivo, il vaccino sia venuto a contatto con strumenti che contengono lattice. Si consiglia ai pazienti sensibili al lattice di consultare il medico prima della somministrazione del vaccino. |
| Mylan Italia S.r.l. | Influvac S* |
Non contiene lattice – non si può escludere la possibilità che, durante il processo produttivo, il vaccino sia venuto a contatto con strumenti che contengono lattice. Si consiglia ai pazienti sensibili al lattice di consultare il medico prima della somministrazione del vaccino. |
| Glaxo Smith Kline Biologicals SA | Fluarix tetra | Non contiene lattice – non utilizzato nel processo produttivo. |
| Sanofi Pasteur Europe | Vaxigrip tetra | Non contiene lattice – non utilizzato nel processo produttivo. |
| Seqirus srl |
Agrippal S1 Fluad Influpozzi subunità Innoflu* Flucelvax tetra |
Non si può escludere che i cappucci copri ago e i cappucci protettivi delle siringhe non contengano lattice. Si consiglia ai pazienti sensibili al lattice di consultare il medico prima della somministrazione del vaccino. |
| AstraZeneca AB | Fluenz tetra* | Non contiene lattice – non utilizzato nel processo produttivo. |
*Vaccini non attualmente in commercio in Italia
I Correlati
Primo caso umano di aviaria in Australia, cresce l'allerta. Bmj: Una grave epidemia di H5N1 è plausibile
Rezza, "L'Italia ha opzionato un vaccino ma manca un piano pandemico"
Covid, per la Fda serve un nuovo vaccino contro la variante JN.1
Il comitato vota all'unanimità la composizone per l'autunno
In Gb 30 ospedali sperimentano vaccini antitumorali personalizzati
Sfruttano la tecnologia a mRna come quelli anti-Covid
Vitiligine, sì dell'AIFA alla rimborsabilità della prima crema efficace
Il farmaco consente la repigmentazione della pelle dei pazienti sia sul viso che sul corpo
Ti potrebbero interessare
Vitiligine, sì dell'AIFA alla rimborsabilità della prima crema efficace
Il farmaco consente la repigmentazione della pelle dei pazienti sia sul viso che sul corpo
Oltre un nuovo farmaco su tre autorizzato per curare i tumori
Secondo i dati del Rapporto Horizon Scanning di Aifa, sono stati autorizzati 89 nuovi medicinali, di cui 48 contenenti nuove sostanze attive, 8 biosimilari, 23 equivalenti e 10 tra medicinali ibridi
Incontro Aifa-Egualia, Nisticò: Al lavoro per assicurare che tutti i farmaci essenziali siano disponibili per i pazienti italiani
“La lotta al fenomeno delle carenze passa anche attraverso il riconoscimento delle necessità di rendere economicamente sostenibili molti farmaci essenziali. Siamo al lavoro su questo aspetto”
Aifa, la carenza di ACE-inibitori in soluzione iniettabile in crisi renale sclerodermica (SRC) non dà rischi per i pazienti
I medicinali a base di enalapril iniettabile non sono disponibili in Italia da oltre vent’anni, in seguito alla revoca dell’Autorizzazione all’Immissione in Commercio (AIC) su rinuncia da parte dell’azienda farmaceutica titolare, nel 2000
Ultime News
Dialogo tra farmacisti ospedalieri, ematologi e oncologi per la gestione dei farmaci ad uso speciale
Cavaliere: i giovani Sifo rappresentano un’anima dinamica e propulsiva della nostra professione
Test di medicina 2024, la graduatoria e i punteggi sono online. Ecco come trovarli
Sono usciti sulla piattaforma Universitaly i risultati dei test di medicina svolti il 28 maggio scorso. Dal 19 giugno si saprà l'esito con nome e cognome
Botox Bar, l’appello di Aiteb: “Rivolgetevi a specialisti esperti e competenti”
Benci (Associazione Terapia Estetica Botulino): “Le iniezioni sono un trattamento medico a tutti gli effetti, non possono essere eseguite frettolosamente”
Opzione donna 2024: le novità che interessano le dottoresse
Per incrociare le braccia occorre aver raggiunto 61 anni (in vari casi possono bastarne 59, come vedremo più avanti) e 35 anni di contributi entro il 31 dicembre 2023








Commenti